Protein adalah makromolekul yang terbentuk
dari polimerisasi peptida-peptida. Peptida merupakan polimerisasi dari asam
amino-asam amino yang berbeda melalui ikatan peptida. Unsur penyusun protein adalah C, H, O dan N.
ASAM AMINO


LATIHAN
1 :
1. Tentukan asam amino - asam amino yang bersifat asam, netral dan basa ?
2. Tulislah
peptidanya, berikan namanya dan tunjukkan ikatan peptida yang
terjadi antara :
a. Glisin – Threonin……… f. Sistein –
alanin
b. Valin –
sistein--------------g. Threonin –
valin
c.
Fenilalanin – serin--------h.
Fenilalanin – leusin
d. Alanin –
leusin--------------i. Sistein –
Serin
e. Valin – glisin-----------------j. Threonin – leusin
SIFAT - SIFAT ASAM AMINO
1. Ion amonium ( - NH3 + ) berfungsi sbg asam dan ion karboksilat ( - COO - ) berfungsi sebagai basa.
Titik isoelektrik (TIE) adalah pH saat as amino bermuatan
0 atau seimbang (-1 & +1).
pH = TIE : bermuatan + dan - (sebagai
ion zwitter)
pH < TIE (pH rendah) : bermuatan
positif (sebagai kation)
pH > TIE (pH tinggi) : bermuatan
negatif (sebagai anion)
2. Bersifat Amfoter
3. Bersifat optis aktif kecuali Glisin
4. Asam amino dapat bergabung asam amino lain membentuk polimer yang disebut Peptida
LATIHAN 2
1. Tulislah
struktur asam amino berikut dalam keadaan pH rendah (<TIE), titik
isoelektrik (TIE) dan pada pH tinggi (>TIE) :
a. Glisin………… e. Serin
b. Valin-------------- f. Sistein
c. Fenilalanin------ h.Threonin
d. Alanin-------------i. Isoleusin
2. Jika pH isoelektrik dari glisin adalah 5,97, tentukanlah gugus fungsi yang bermuatan pada pH 3 dan pH 6,8 ?
3. Asam amino X mempunyai pH isoelektrik sebesar 7,64, tentukan muatan parsial rata-rata pada pH 3 ?
4. Titik isoelektrik Fenilalanin adalah 5,5. Gambarkan struktur spesi fenilalanin dalam larutan pada pH berikut :
a) 3,0--------b) 5,5--------c) 8,0
5. Titik isoelektrik dari alanin ( NH2-CH(CH3)-COOH ) adalah 6. Pada pH berapakah, spesi NH2-CH(CH3)-COO – dominan ?
STRUKTUR PROTEIN
1. Struktur PRIMER : urut-urutan asam amino dalam rantai polipeptida yang menyusun protein
2. Struktur SEKUNDER : Spiral (Alpha Heliks)akibat adanya interaksi sekunder (misal ikatan NH2 dan R antar asam amino)
3. Struktur TERTIER : bentuk tiga dimensi dari suatu protein yang terbentuk akibat interaksi antara struktur sekunder satu dengan yang lain melalui ikatan hidrogen, ionik dll (hanya terdiri dari satu subunit polipeptida)
4. Struktur KWARTERNER : Struktur yang melibatkan beberapa peptida sehingga membentuk protein.
SIFAT-SIFAT
PROTEIN
1. Sukar larut dalam air
2. Dapat mengalami koagulasi oleh
pemanasan dan
elektrolit
3. Bersifat amfoter
4. Dapat mengalami denaturasi (kerusakan) : hilangnya fungsi biologis suatu protein karena adanya perubahan struktur protein. Denaturasi protein dapat terjadi karena adanya pengaruh pemanasan, penambahan asam, penambahan basa, penambahan garam dan agitasi mekanik.
FUNGSI PROTEIN
1. Enzim/biokatalis
2. Protein transpor
3. Contoh: hemoglobin.
4. Protein
nutrien/makanan
5. Protein
kontraktil Contoh: aktin dan miosin pada kontraksi otot.
6. Protein
struktur Contoh: protein rambut dan kuku.
7. Protein
pertahananContoh: antibodi
8. Protein pengatur contoh: hormon
LATIHAN 3 :
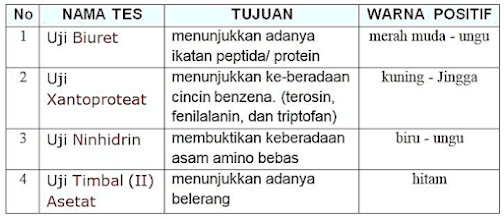
1. Perhatikan data hasil percobaan uji protein
berikut. Berdasarkan data tersebut maka protein yang mengandung gugus
inti benzena dan belerang adalah ….
2. Protein yang mengandung leusin banyak ditemukan
dalam kacang-kacangan. Jika diketahui kacang polong mengandung protein (Mr =
1.600) yang hanya terbentuk dari monomer asam amino leusin melalui reaksi
kondensasi, maka berapakah banyak leusin yang menyusun protein tersebut?
(Diketahui Mr leusin = 131)
3. Jika 20 asam amino alanin (H3C-CH(NH2)-CO2 H)
terpolimerisasi kondensasi membentuk protein, maka pernyataan berikut ini yang
benar adalah ...(Mr alanin = 89)
(1) akan dihasilkan 20 molekul air
(2) bersifat optis aktif
(3) akan dihasilkan protein dengan berat molekul 1780
(4) terbentuk protein yang dapat diuji dengan reagen Biuret
4. Suatu polipeptida (Mr = 1.305) terbentuk
dari monomer asam amino valin (Mr = 117) melalui polimerisasi kondensasi. Jika
polipeptida tersebut dihidrolisis dengan bantuan enzim tertentu, Berapakah
jumlah monomer asam amino valin yang dihasilkan ?
5. Suatu polimer polialanin terbentuk dari polimerisasi alanin. Jika Ar C=12, O=16, N=14, H=1, dan massa molekul relatif polialanin sebesar = 728, Tentukan jumlah molekul alanin ?
6. Nama IUPAC dari asam amino fenil alanin berikut adalah ….
7. Histidin merupakan salah satu asam
amino penyusun protein. Struktur histidin ditunjukkan oleh gambar di bawah ini, Tentukan
















 div>
div>









Tidak ada komentar:
Posting Komentar