Bilangan kuantum adalah bilangan yang
menyatakan kedudukan atau posisi elektron dalam atom. Bilangan kuantum
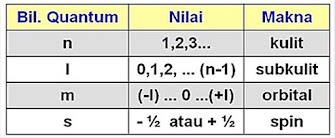
dinyatakan dalam 4 jenis berikut :
1. Bilangan Kuantum Utama (n)
Menyatakan tingkat
energi utama elektron suatu atom atau menunjukkan kulit atom.
n=1 (kulit K),
n=2 (kulit L),
n=3 (kulit M) dst…
2. Bilangan Kuantum Azimut (l)
menyatakan bentuk
orbital atau subkulit suatu atom. Nilai dari bilangan ini bisa menunjukkan
subkulit s, p, d, atau f. Nilai l = 0 s.d (n-1)
l = 0 (subkulit s)
l = 1 (subkulit p)
l = 2 (subkulit d)
l = 3 (subkulit f)
3. Bilangan Kuantum Magnetik (m)
Menyatakan jumlah
orbital yang menyusun subkulit dan orientasi dari orbital tersebut. Nilai m = -
l s.d +l
Contoh: jika l = 2 (subkulit d) maka m = -2, -1, 0 +1, +2 dengan demikian jumlah orbital = 5,
yang dilambangkan
dengan kotak sebanyak 5.
|
|
|
|
|
|
|
-2 |
-1 |
0 |
+1 |
+2 |
4. Bilangan Kuantum Spin (s)
Menyatakan arah
rotasi elektron dalam orbital. Nilai s hanya bisa - ½ atau +½ saja. Jika nilainya positif, menunjukkan
bahwa spin arahnya ke atas dan dilambangkan simbol panah ke atas (↑). Dan jika
s negatif, berarti spin ke arah bawah, lambang panah ke bawah (↓).
Panah merah menunjukkan posisi elektron terakhir, dimana m = +1, s = - ½
Contoh soal :
Tentukan ke-4 bilangan kuantum elektron terakhir pada aton S (no. atom 16)
LATIHAN SOAL :
1. Tentukan keempat harga bilangan kuantum
elektron terakhir dari atom-atom dengan nomor :
a. 18 P---- ----d. 29 Q--
---g. 34 R
b. 39 S-- ---e. 47T--------h. 50 U
c. 55 V-- -----f. 73 W---- i. 37 X
2. Tentukan keempat harga bilangan kuantum
elektron terakhir dari ion-ion dengan nomor:
a. 17 A -1-----d. 25 B +3-----g. 29 C +1
b. 27 D +3----e.33 E- 3-------h. 44 F +4
c. 53 G -1-----f. 56 H +2------i. 65 I +2
3. Tentukan konfigurasi elektron, nomor atom, golongan dan periode dari atom-atom yang mempunyai 4 bilangan kuantum elektron terakhirnya sebagai berikut :
|
A |
n = 4 |
l = 1 |
m = -1 |
s = - ½ |
|
B |
n = 3 |
l = 2 |
m = +2 |
s = - ½ |
|
C |
n = 4 |
l = 2 |
m = -2 |
s = +½ |
|
D |
n = 5 |
l = 0 |
m = 0 |
s = - ½ |
|
E |
n = 3 |
l = 1 |
m = +1 |
s = +½ |
4. Ion X+2 mempunyai bilangan kuantum elektron terakhir : n = 5, l = 1, m = -1, s = +1/2, tentukan konfigurasi elektron, nomor atom, golongan dan periode atom X ?
5. Ion Y-3 mempunyai bilangan kuantum elektron terakhir : n = 4, l = 1, m = -1, s = -1/2, tentukan konfigurasi elektron dan nomor atom golongan dan periode atom Y ?
6. Suatu elektron memiliki harga bilangan kuantum utama (n) = 4. Tentukan bilangan kuantum yang mungkin lainnya !
















 div>
div>


semoga kesehatan rezeki kesuksesan menyertai kita semua amiennn...
BalasHapusaamiin !
Hapusaamiin bu!
Hapus